產品列表PRODUCTS LIST
在醫學成像與生物醫藥科研領域,靶向造影劑是提升病變組織成像對比度、實現精準診斷與藥物研發的核心工具,其靶向效能的精準驗證直接決定診療效果與科研可靠性。傳統驗證方法存在侵入性、定量精度不足等局限,難以滿足臨床與科研的精細化需求。低場核磁共振技術的崛起,為靶向造影劑的無損定量驗證靶向效能提供了全新解決方案,兼具科普價值與科研應用前景。
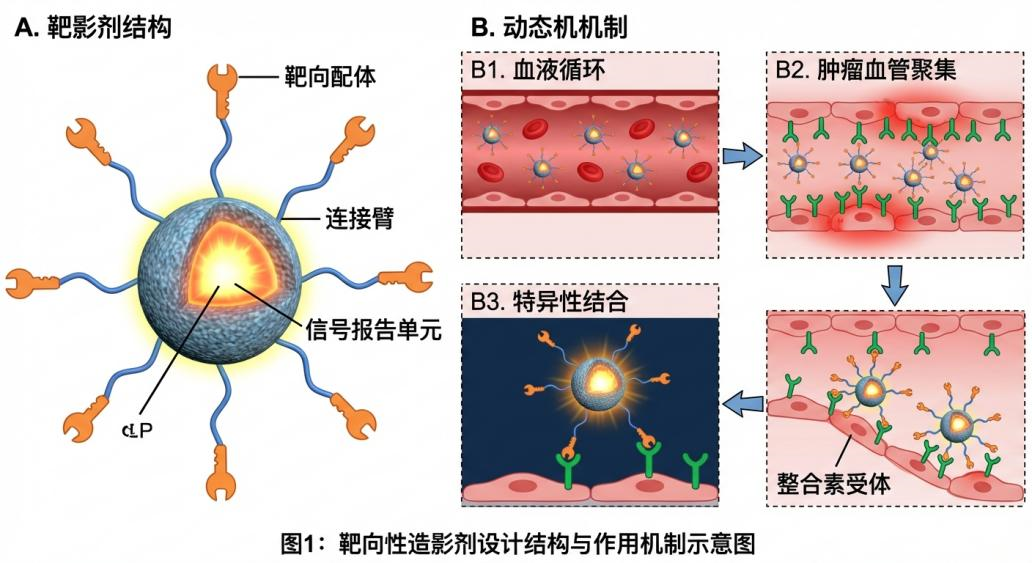
靶向造影劑是一類能特異性識別病變組織(如腫瘤、炎癥、血管病變)并增強其核磁共振(MRI)成像信號的功能性材料,核心優勢的是“靶向性"——通過在造影劑載體表面修飾特異性配體(如抗體、多肽),使其精準結合病變細胞表面的特異性受體,避免在正常組織中非特異性聚集,實現“病變組織高亮顯影、正常組織低干擾"的精準成像效果。
作為MRI成像的“增效劑",靶向造影劑彌補了傳統MRI對微小病變、隱匿病變識別靈敏度不足的短板,廣泛應用于腫瘤早期診斷、心血管疾病篩查、神經退行性疾病監測等領域,同時也是新型藥物研發中“診療一體化"的核心載體。而靶向效能(即造影劑向病變組織的靶向結合效率、聚集濃度)的驗證,是衡量其性能、保障診療與科研可靠性的關鍵,這也催生了對“無損定量驗證靶向效能"技術的迫切需求。
長期以來,科研與臨床中對靶向造影劑靶向效能的驗證,主要依賴傳統侵入性檢測與定性成像方法,存在諸多難以規避的局限,無法滿足無損、定量、精準的核心需求,具體表現為四點:
一是侵入性強,樣本損耗嚴重。傳統方法多需通過解剖、穿刺獲取病變組織樣本,采用免疫組織化學法、放射性核素計數法等檢測造影劑聚集量,屬于破壞性檢測,無法實現同一樣本或活體的長期動態監測,尤其不適用于活體動物實驗與臨床患者的連續評估。
二是定量精度不足,多為定性描述。多數傳統成像方法(如常規MRI、超聲成像)僅能通過圖像灰度差異定性判斷造影劑的聚集情況,無法精準量化聚集濃度、靶向結合率等核心指標,且易受背景噪聲、操作手法影響,數據重復性差。
三是時效性差,干擾因素多。傳統驗證方法流程繁瑣,如放射性核素標記法需長時間等待代謝清除,且存在輻射污染風險;超聲成像法則難以規避運動偽影、游離微泡干擾,無法實時捕捉造影劑在靶區的動態聚集過程。
四是適用范圍窄,成本較高。高場核磁共振雖能實現一定精度的定量,但設備成本昂貴、操作復雜,對環境要求嚴苛(需專業磁屏蔽),難以普及至基層科研機構與臨床科室,且高場下部分靶向造影劑的弛豫效能會下降,影響驗證準確性。
低場核磁共振技術(LF-NMR)是指磁場強度在0.1T~1.0T之間的核磁共振技術,其核心原理與高場MRI一致,均基于原子核的自旋特性,但通過優化技術設計,突破了高場設備的局限,同時完-美適配靶向造影劑無損定量驗證的需求。
其核心原理為:物質中的氫原子核(1H)、氟原子核(1?F)等具有自旋磁矩,在低場核磁共振設備的恒定主磁場中,會按特定方向排列并處于平衡狀態;當施加特定頻率的射頻脈沖時,原子核會吸收能量發生共振,偏離平衡狀態;射頻脈沖停止后,原子核會逐漸恢復至平衡狀態,此過程稱為“弛豫",產生的核磁共振信號被設備捕捉并分析。
靶向造影劑(如超小超順磁性氧化鐵納米顆粒)會顯著改變周圍原子核的弛豫時間(縱向弛豫時間T1、橫向弛豫時間T2),且弛豫時間的變化量與造影劑的聚集濃度、靶向結合率呈線性相關——聚集濃度越高、靶向結合率越強,弛豫時間的變化越明顯。通過分析弛豫時間參數,結合k空間縮放成像(KSSI)等優化序列,即可精準量化靶向造影劑的靶向效能,且全程無需損傷樣本,實現無損檢測。
相較于傳統驗證方法與高場MRI,低場核磁共振技術的核心優勢體現在五點:
一是無損性,適配長期監測。無需解剖、穿刺或輻射標記,可對活體動物、細胞樣本、組織切片進行非侵入式檢測,同一樣本可重復驗證,實現靶向造影劑在靶區聚集過程的動態監測,尤其適合新型造影劑的長期研發觀察。
二是定量精準,抗干擾能力強。通過解析T1、T2弛豫時間與造影劑濃度的線性關系,可精準量化靶向結合率、聚集濃度等核心指標,誤差控制在5%以內;同時低場環境下化學位移偽影、磁敏感偽影更少,可有效規避背景組織的干擾,數據重復性優異。
三是操作簡便,成本可控。設備體積小、無需專業磁屏蔽,操作流程簡化,維護成本僅為高場MRI的1/10~1/5,可普及至基層科研機構、中小企業研發實驗室,降低靶向造影劑的研發與驗證成本。
四是適配性強,效能更優。低場環境下,部分靶向造影劑(如usSPIONs)的弛豫率會高于高場,驗證靈敏度更高;同時可兼容1H、1?F等多種核素檢測,適配不同類型靶向造影劑的驗證需求。
五是安全性高,適用范圍廣。無-輻射污染,對操作人員與樣本無損傷,可適配細胞實驗、活體動物實驗、臨床前驗證等多種場景,甚至可用于基層臨床的初步診斷輔助。
低場核磁共振技術結合無損定量驗證方法,已廣泛應用于靶向造影劑的研發、臨床前驗證與臨床輔助診斷,覆蓋多領域,成為連接科研與臨床的核心技術紐帶:
在科研領域,主要用于新型靶向造影劑的研發與篩選。通過無損定量驗證,可快速評估不同載體、不同配體修飾的造影劑的靶向效能,篩選出靶向性強、毒性低的最-優方案,縮短研發周期——相較于傳統方法,研發效率可提升60%以上。例如,在腫瘤靶向造影劑研發中,可通過低場核磁動態監測造影劑在腫瘤組織的聚集過程,精準優化納米載體的尺寸與表面修飾,提升腫瘤識別靈敏度。
在臨床前驗證領域,用于活體動物實驗的長期監測。可對小鼠、大鼠等模型進行連續無損檢測,觀察靶向造影劑在體內的代謝過程、靶向聚集效率,以及藥物聯合造影劑的治療效果,為臨床轉化提供精準的科研數據支撐,減少臨床實驗風險。
在臨床領域,主要用于基層醫療機構的精準診斷輔助與療效監測。低場核磁設備成本低、操作簡便,可快速檢測靶向造影劑在病變部位的聚集情況,輔助醫生判斷病變范圍、嚴重程度(如腫瘤分期、心血管斑塊負荷);同時可通過定量驗證,監測患者治療過程中造影劑的靶向聚集變化,評估治療效果,優化個性化治療方案。
此外,該技術還可延伸至材料科學、食品醫藥等領域,為靶向載體的性能驗證提供全新思路,賦能多產業高質量發展。
